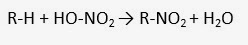Dalam bab ini akan dibahas tentang tata n
ama, sifat-sifat fisika dan kimia senyawa organik golongan alkana, yaitu salah satu jenis dari kelompok hidrokarbon alifatik. Senyawa hidrokarbon adalah senyawa organik yang molekulnya tersusun dari atom-atom karbon dan hidrogen. Terdapat 3 golongan senyawa yang termasuk hidrokarbon yaitu, hidrokarbon alifatik (alkana, alkena, alkuna), hidokarbon alisiklik (siklo alkana, siklo alkena), dan hidrokarbon aromatik (benzena dan turunannya). Dalam hidrokarbon alifatik terdapat dua macam golongan yaitu hidrokarbon alifatik jenuh dan hidrokarbon alifatik tidak jenuh.
Ciri- ciri hidrokarbon alifatik jenuh adalah hanya memiliki ikatan tunggal di antara rantai-rantai karbonnya, dan rangkaian atom-atom karbon tersebut merupakan rantai terbuka ( ujung-ujung rantainya tidak saling bertemu). Karena dalam molekul alkana ikatan antara atom-atom karbonnya semuanya berupa ikatan tunggal, maka alkana merupakan senyawa hidrokarbon alifatik jenuh.
Istilah alifatik berasal dari kata Yunai aleiphar yang berarti lemak atau minyak. Bahwa alkana dinyatakan sebagai hidrokarbon alifatik karena sifat fisika suku-suku tinggi alkana menyerupai sifat fisika molekul berantai panjang yang terdapat dalam lemak hewan dan minyak tumbuhan.
I. Struktur Alkana
Rumus umum molekul alkana adalah CnH2n+2 . Bentuk molekul metana adalah tetrahedron dan semua sudut ikatan H-C-H 109,5. Semua atom karbon dalam etana juga tetrahedron dan semua sudut ikatannya mendekati 109,5.
II. Keisomeran Struktur Dalam Alkana
Senyawa-senyawa yang mempunyai rumus molekul sama tetapi rumus strukturnya berbeda(dalam hal cara terikatnya atom-atom dalam molekul) disebut isomer-isomer struktur. Misalnyua alkana dengan rumus molekul C4H10 mempunyai dua buah isomer struktur, yang masing-masing diberi nama butana dan 2-metilpropana (isobutana). Isobutana dan 2-metilpropana adalah dua senyawa yang berbeda strukturnya dan mempunyai sifat fisika dan kimia yangberbeda pula.
III. Tata Nama Alkana
Sistem IUPAC
Secara ideal setiap senyawa organik seharusnya mempunyai satu nama yang memberikan gambaran secara jelas tetntang strukturnya, dan sebaliknya dari nama itu pula dapat digambarkan rumus struktur senyawa tersebut. Untuk memenuhi ketentuan tersebut oleh suatu badan bernama International Union of Pure and Applied Chemistry (IUPAC) telah disusun seperangkat peraturan untuk memberi nama senyawa organik.
pemberian nama pada alkana dengan rantai tak bercabang menurut sistem IUAPC terdiri dari dua bagian, yaitu : (1) awalan yang emnyatakan jumlah atom karbon dalam rantai, dan (2) akhiran -ana untuk menunjukkan bahwa senyawanya berupa hidrokarbon alifatik jenuh. Awalan yang digunakan untuk menyatakan jumlah 1 sampai dengan 20 atom C dapat dilihat pada tabel sebelumnya.
Untuk pemberian rantai alkana bercabang terdiri dari dua bagian yaitu nama induk yang menunjukkan atom-atom karbon yang membentuk rantai utama (rantai karbon terpanjang), dan nama cabang yang menunjukkan gugus yang terikat pada rantai utama.
Contoh CH3-CH2-CH2-CH(CH3)-CH2-CH3
Satu gugus yang diturunkan dari suatu alkana dengan mengurangi satu atom H disebut gugus alkil. Gugus alkil umumnya dilambangkan dengan -R, dan diberi nama dengan mengganti akhiran -ana pada alkana asalnya dengan akhiran -il
Aturan-aturan pemberian nama alkana menurut sistem IUPAC :
Dalam sistem nama umum atau trivial yang lama, nama alkana ditentukan oleh jumlah atom karbon tanpa memperhatikan susunan atom-atom karbon tersebut. Tiga suku pertama alkana berturut-turut diberi nama metana, etana, dan propana,. Semua senyawa yang mempunyai rumus molekul C4H10 disebut butana. Alkana tak bercabang yang mempunyai atom karbon lebih dari 3 diberi awalan normal (n). Awalan iso- menunjukkan adanya gugus -C(CH3)3 pada ujung rantai. Sistem nama TRIVIAL ini biasanya digunakan untuk struktur-struktur alkana dengan rantai yang sederhana, jika rantai dari suatu alkana tersebut cukup kompleks maka digunakan sistem nama IUPAC.
IV. Klasifikasi Atom-atom Karbon dan Hidrogen
Atom karbon dibedakan menjadi 4 yaitu: primer, sekunder, tersier, dan kuartener. Atom karbon primer adalah atom karbon yang mengikat 1 atom karbon yang lain. Atom karbon sekunder mengikat 2 atom karbon yang lain, sedangkan atom karbon tersier dan kuartener berturut-turur mengikat 3 dan 4 atom karbon yang lain.
Untuk atom hidrogen dibedakan menjadi 3 yaitu primer, sekunder, dan tersier tergantung pada jenis atom karbon yang mengikatnya. Atom hidrogen yang terikat pada atom karbon primer disebut atom hidrogen primer, atom hidrogen yang terikat pada atom karbon sekunder disebut atom hidrogen sekunder, dan selanjutnya. d
V. Konformasi Alkana
Bila alkana yang mempunyai 2 atau lebih atom karbon diputar mengelilingi garis ikatan karbon-karbonmaka akan menghasilkan tatanan 3 dimensi yang berbeda-beda. Setiap tatanan 3 dimensi atom-atom yang dihasilkan oleh rotasi pada sumbu ikatan tunggal disebut konformasi.
Contohnya, molekul etana yang digambarkan dengan proyeksi Newman. Yang dimaksud gambar proyeksi Newman adalah gambar molekul yang diperoleh dengan cara memandang molekul tersebut dari arah sumbu ikatan karbon-karbon.
Apabila dilakukan pemutaran mengelilingi sumbu ikatan C-C berturut-turut sebesar 60, 120, 180, 240, dan 300 derajat maka diperoleh konformasi sebagai berikut
Apabila diamati keenam konformer tersebut ternyata hanya terdapat 2 konformer yang ekstrem yaitu konformasi goyang (staggered) dan eklips (eclipsed). Konformasi "goyang" dan "eklips" ditunjukkan oleh gambar dibawah ini
Pada konformasi "goyang", ketiga ikatan C-H pada atom karbon yang satu berjauhan dengan tiga ikatan C-H pada atom karbon yang berdampingan. Sebaliknya pada konformasi "eklips", ketiga ikatan C-H pada atom karbon yang satu berdekatan dengan tiga ikatan C-H atom karbon yang berdampingan.
VI. Sifat-sifat Fisika Alkana
1. Alkana yang memiliki berat molekul rendah (metana, etana, propana, dan butana) pada suhu kamar dan tekanan atmosfer berwujud gas. Alkana yang memiliki 5-17 atom C berwujud cair dan selebihnya berwujud padat. Titik didih dan titik leleh alkana makin tinggi bila berat molekulnya bertambah.
2. Alkana adalah senyawa nonpolar, dan gaya antar molekulnya adalah gaya van der waals. Oleh karena itu titik leleh dan titik didih alkana lebih rendah daripada senyawa semipolar atau senyawa polar yang berat molekulnya hampir sama.
VII. Reaksi-reaksi pada Alkana
Alkana sangat tidak reaktif terhadap sebagian besar peraksi. Alkana merupakan senyawa nonpolar dan hanya memiliki ikatan sigma-sigma yang kuat.
1. Reaksi Oksidasi
Alkana bila bereaksi dengna oksigen dalam jumlah yang memadai (teroksidasi sempurna) membentuk CO2 dan H2O disertai pembebasan panas.
2. Reaksi Halogenasi
Alkana bereaksi dengan halogen di bawah pengaruh panas atau sinar ultraviolet.
Melalui eksperimen, Markovnikov (tahun 1875) memperoleh bukti bahwa dalam reaksi substitusi terdapat perbedaan laju reaksi substitusi di antara atom-atom H dalam alkana, yaitu H3>H2>H1. Pada halogenasi (kecuali fluorinasi), ternyata bahwa kereaktifannya dalam reaksi substitusi adalah klorin > brom > iodin.
3. Reaksi nitrasi
Reaksi alkana dengan HNO3 pada suhu 150-475 derajat celcius mengakibatkan terjadinya substitusi atom H pada alkana oleh gugus -NO2 (gugus nitro). Reaksi substitusi semacam ini dinamakan reaksi nitrasi
Seperti halnya pada halogenasi, atom-atom H dalam alkana berbeda laju reaksinya dalam nitrasi sehingga hasil nitrasi cenderung membbentuk campuran.
Contoh : propana + asam nitrat akan menghasilkan campuran 1- nitopropana dan 2-nitropropana
4. Reaksi sulfonasi
Reaksi alkana dengan asam sulfat berasap (oleum) menghasilkan asam alkana sulfonat.
Dalam reaksi di atas terjadi substitusi satu atom H pada alkana oleh gugus -SO3H dan substitusi ini dinamakan dengan sulfonasi. Dalam reaksi sulfonasi terbukti bahwa laju substitusi H3>H2>H1.
5. Isomerisasi
Pada beberapa lakana dalam kondisi tertentu dapat terjadi isomerisasi
VIII. Pembuatan Alkana
Pembuatan alkana dapat dibuat dengan beberapa cara diantaranya adalah :
1. Hidrogenasi alkena
Alkena direaksikan dengan hidrogen dalam katalis Pd/Pt/Ni dapat menghasilkan alkena
2. Hidrolisis pereaksi Grignard
Jika suatu alkil halida direaksikan dengan logam Mg dalam eter kering maka akan dihasilkan sebuah peraksi grignard yang jika dihidrolisis akan menghasilkan suatu alkana
3. Reaksi Wurtz
Reaksi Wurtz biasa digunakan untuk penggandengan alkil halida dengan senyawa organologam.
IX. Sumber-sumber Alkana
Sumber-sumber Alkana yang terdapat di alam adalah bahan bakar fosil yang meliputi gas alam, minyak bumi, dan batubara.
Semoga bermanfaat :)
Tunggu untuk posting materi selanjutnya..
Ciri- ciri hidrokarbon alifatik jenuh adalah hanya memiliki ikatan tunggal di antara rantai-rantai karbonnya, dan rangkaian atom-atom karbon tersebut merupakan rantai terbuka ( ujung-ujung rantainya tidak saling bertemu). Karena dalam molekul alkana ikatan antara atom-atom karbonnya semuanya berupa ikatan tunggal, maka alkana merupakan senyawa hidrokarbon alifatik jenuh.
Istilah alifatik berasal dari kata Yunai aleiphar yang berarti lemak atau minyak. Bahwa alkana dinyatakan sebagai hidrokarbon alifatik karena sifat fisika suku-suku tinggi alkana menyerupai sifat fisika molekul berantai panjang yang terdapat dalam lemak hewan dan minyak tumbuhan.
I. Struktur Alkana
Rumus umum molekul alkana adalah CnH2n+2 . Bentuk molekul metana adalah tetrahedron dan semua sudut ikatan H-C-H 109,5. Semua atom karbon dalam etana juga tetrahedron dan semua sudut ikatannya mendekati 109,5.
II. Keisomeran Struktur Dalam Alkana
Senyawa-senyawa yang mempunyai rumus molekul sama tetapi rumus strukturnya berbeda(dalam hal cara terikatnya atom-atom dalam molekul) disebut isomer-isomer struktur. Misalnyua alkana dengan rumus molekul C4H10 mempunyai dua buah isomer struktur, yang masing-masing diberi nama butana dan 2-metilpropana (isobutana). Isobutana dan 2-metilpropana adalah dua senyawa yang berbeda strukturnya dan mempunyai sifat fisika dan kimia yangberbeda pula.
III. Tata Nama Alkana
Sistem IUPAC
Secara ideal setiap senyawa organik seharusnya mempunyai satu nama yang memberikan gambaran secara jelas tetntang strukturnya, dan sebaliknya dari nama itu pula dapat digambarkan rumus struktur senyawa tersebut. Untuk memenuhi ketentuan tersebut oleh suatu badan bernama International Union of Pure and Applied Chemistry (IUPAC) telah disusun seperangkat peraturan untuk memberi nama senyawa organik.
pemberian nama pada alkana dengan rantai tak bercabang menurut sistem IUAPC terdiri dari dua bagian, yaitu : (1) awalan yang emnyatakan jumlah atom karbon dalam rantai, dan (2) akhiran -ana untuk menunjukkan bahwa senyawanya berupa hidrokarbon alifatik jenuh. Awalan yang digunakan untuk menyatakan jumlah 1 sampai dengan 20 atom C dapat dilihat pada tabel sebelumnya.
Untuk pemberian rantai alkana bercabang terdiri dari dua bagian yaitu nama induk yang menunjukkan atom-atom karbon yang membentuk rantai utama (rantai karbon terpanjang), dan nama cabang yang menunjukkan gugus yang terikat pada rantai utama.
Contoh CH3-CH2-CH2-CH(CH3)-CH2-CH3
Satu gugus yang diturunkan dari suatu alkana dengan mengurangi satu atom H disebut gugus alkil. Gugus alkil umumnya dilambangkan dengan -R, dan diberi nama dengan mengganti akhiran -ana pada alkana asalnya dengan akhiran -il
 |
| Nama dan Rumus molekul 20 suku pertama alkana dengan rantai tak bercabang |
- Alkana tidak bercabang diberi nama seperti pada tabel pertama
- Untuk alkana yang rantainyua bercabang, nama senyawa induknya adalah nama alkana yang jumlah atom C-nya sesuai dengan rantai atom karbon yang terpanjang. Rantai atom karbon yang terpanjang tersebut dinyatakan sebagai rantai utama.
- Gugus- gugus yang terikat pada rantai utama disebut subtituen, dan setiap subtituen mempunyai satu nama dan satu nomor. Nomor tersebut menunjukkan nomor atom karbon dalam rantai utama yang mengikat subtituen.
- Jika terdapat lebih dari satu subtituen yang sama, maka nomor masing-masing atom karbon rantai utama yang mengikat suntituen tersebut harus dituliskan. Jumlah subtituen ditunjukkan dengan awalan di-, tri-, tetra-, penta-, heksa-, dan seterusnya, yang berturut-turut menyatakan jumlah subtituen sebanyak dua, tiga, empat, lima, enam dan seterusnya.
- Jika suatu alkana bercabang hanya memiliki sebuat subtituen, maka penomoran rantai utama dimulai dari ujung rantai yang memberi nomor rendah pada subtituen tersebut.
- Jika terdapat dua atau lebih subtituen yang sama, maka pernomoran rantai utama dari ujung yang meberikan nomor rendah pada subtituen yang posisinya terdekat dengan ujung rantai tersebut.
- Jika terdapat dua atau lebnih subtituen yang berbeda, maka dalam penulisan namanya harus disusun berdasarkan urutan abjad huruf pertama nama subtituen. Penomoran rantai utama dimulai dari ujung yang menghasilkan nomor yang lebih rendah bagi subtituen dengan urutan abjad lebih awal.
- Awalan di-, tri-, tetra-, dan seterusnya tidak perlu diperhatikan dalam penentuan urutan abjad
- Awalan-awalan yang diikuti dengan tanda hubung seperti sekunder (sek-), tersier (ters-) tidak perlu diperhatikan dalam penentuan urutan abjad, sedangkan awalan iso dan neo tidak perlu dipisahkan dengantanda hubung tetapi harus diperhatikan dalam penentuan urutan abjad.
Dalam sistem nama umum atau trivial yang lama, nama alkana ditentukan oleh jumlah atom karbon tanpa memperhatikan susunan atom-atom karbon tersebut. Tiga suku pertama alkana berturut-turut diberi nama metana, etana, dan propana,. Semua senyawa yang mempunyai rumus molekul C4H10 disebut butana. Alkana tak bercabang yang mempunyai atom karbon lebih dari 3 diberi awalan normal (n). Awalan iso- menunjukkan adanya gugus -C(CH3)3 pada ujung rantai. Sistem nama TRIVIAL ini biasanya digunakan untuk struktur-struktur alkana dengan rantai yang sederhana, jika rantai dari suatu alkana tersebut cukup kompleks maka digunakan sistem nama IUPAC.
IV. Klasifikasi Atom-atom Karbon dan Hidrogen
Atom karbon dibedakan menjadi 4 yaitu: primer, sekunder, tersier, dan kuartener. Atom karbon primer adalah atom karbon yang mengikat 1 atom karbon yang lain. Atom karbon sekunder mengikat 2 atom karbon yang lain, sedangkan atom karbon tersier dan kuartener berturut-turur mengikat 3 dan 4 atom karbon yang lain.
Untuk atom hidrogen dibedakan menjadi 3 yaitu primer, sekunder, dan tersier tergantung pada jenis atom karbon yang mengikatnya. Atom hidrogen yang terikat pada atom karbon primer disebut atom hidrogen primer, atom hidrogen yang terikat pada atom karbon sekunder disebut atom hidrogen sekunder, dan selanjutnya. d
V. Konformasi Alkana
Bila alkana yang mempunyai 2 atau lebih atom karbon diputar mengelilingi garis ikatan karbon-karbonmaka akan menghasilkan tatanan 3 dimensi yang berbeda-beda. Setiap tatanan 3 dimensi atom-atom yang dihasilkan oleh rotasi pada sumbu ikatan tunggal disebut konformasi.
Contohnya, molekul etana yang digambarkan dengan proyeksi Newman. Yang dimaksud gambar proyeksi Newman adalah gambar molekul yang diperoleh dengan cara memandang molekul tersebut dari arah sumbu ikatan karbon-karbon.
 | ||
| Proyeksi Newman molekul etana |
Apabila diamati keenam konformer tersebut ternyata hanya terdapat 2 konformer yang ekstrem yaitu konformasi goyang (staggered) dan eklips (eclipsed). Konformasi "goyang" dan "eklips" ditunjukkan oleh gambar dibawah ini
Pada konformasi "goyang", ketiga ikatan C-H pada atom karbon yang satu berjauhan dengan tiga ikatan C-H pada atom karbon yang berdampingan. Sebaliknya pada konformasi "eklips", ketiga ikatan C-H pada atom karbon yang satu berdekatan dengan tiga ikatan C-H atom karbon yang berdampingan.
VI. Sifat-sifat Fisika Alkana
1. Alkana yang memiliki berat molekul rendah (metana, etana, propana, dan butana) pada suhu kamar dan tekanan atmosfer berwujud gas. Alkana yang memiliki 5-17 atom C berwujud cair dan selebihnya berwujud padat. Titik didih dan titik leleh alkana makin tinggi bila berat molekulnya bertambah.
2. Alkana adalah senyawa nonpolar, dan gaya antar molekulnya adalah gaya van der waals. Oleh karena itu titik leleh dan titik didih alkana lebih rendah daripada senyawa semipolar atau senyawa polar yang berat molekulnya hampir sama.
VII. Reaksi-reaksi pada Alkana
Alkana sangat tidak reaktif terhadap sebagian besar peraksi. Alkana merupakan senyawa nonpolar dan hanya memiliki ikatan sigma-sigma yang kuat.
1. Reaksi Oksidasi
Alkana bila bereaksi dengna oksigen dalam jumlah yang memadai (teroksidasi sempurna) membentuk CO2 dan H2O disertai pembebasan panas.
2. Reaksi Halogenasi
Alkana bereaksi dengan halogen di bawah pengaruh panas atau sinar ultraviolet.
Melalui eksperimen, Markovnikov (tahun 1875) memperoleh bukti bahwa dalam reaksi substitusi terdapat perbedaan laju reaksi substitusi di antara atom-atom H dalam alkana, yaitu H3>H2>H1. Pada halogenasi (kecuali fluorinasi), ternyata bahwa kereaktifannya dalam reaksi substitusi adalah klorin > brom > iodin.
3. Reaksi nitrasi
Reaksi alkana dengan HNO3 pada suhu 150-475 derajat celcius mengakibatkan terjadinya substitusi atom H pada alkana oleh gugus -NO2 (gugus nitro). Reaksi substitusi semacam ini dinamakan reaksi nitrasi
Seperti halnya pada halogenasi, atom-atom H dalam alkana berbeda laju reaksinya dalam nitrasi sehingga hasil nitrasi cenderung membbentuk campuran.
Contoh : propana + asam nitrat akan menghasilkan campuran 1- nitopropana dan 2-nitropropana
4. Reaksi sulfonasi
Reaksi alkana dengan asam sulfat berasap (oleum) menghasilkan asam alkana sulfonat.
Dalam reaksi di atas terjadi substitusi satu atom H pada alkana oleh gugus -SO3H dan substitusi ini dinamakan dengan sulfonasi. Dalam reaksi sulfonasi terbukti bahwa laju substitusi H3>H2>H1.
5. Isomerisasi
Pada beberapa lakana dalam kondisi tertentu dapat terjadi isomerisasi
VIII. Pembuatan Alkana
Pembuatan alkana dapat dibuat dengan beberapa cara diantaranya adalah :
1. Hidrogenasi alkena
Alkena direaksikan dengan hidrogen dalam katalis Pd/Pt/Ni dapat menghasilkan alkena
2. Hidrolisis pereaksi Grignard
Jika suatu alkil halida direaksikan dengan logam Mg dalam eter kering maka akan dihasilkan sebuah peraksi grignard yang jika dihidrolisis akan menghasilkan suatu alkana
3. Reaksi Wurtz
Reaksi Wurtz biasa digunakan untuk penggandengan alkil halida dengan senyawa organologam.
IX. Sumber-sumber Alkana
Sumber-sumber Alkana yang terdapat di alam adalah bahan bakar fosil yang meliputi gas alam, minyak bumi, dan batubara.
Semoga bermanfaat :)
Tunggu untuk posting materi selanjutnya..